Com estem guanyant la guerra contra el càncer
La medicina de precisió, la immunoteràpia i el coneixement de les vies que impulsen la metàstasi dibuixen el marc estratègic de les teràpies oncològiques de present i de futur immediat

BarcelonaEl periodista i escriptor nord-americà Clifton Leaf es preguntava l’any 2004 si estàvem guanyant la guerra contra el càncer o si l’estratègia seguida fins aleshores era la correcta. En un celebrat article publicat a la revista Fortune, el periodista feia una anàlisi econòmica, repassava la història de la recerca en càncer i avaluava la inversió pública i privada des que el president Richard Nixon va signar l’Acta Nacional contra el Càncer l’any 1971. La conclusió de Leaf era que les teràpies disponibles en aquell moment no justificaven tanta despesa.
L’opinió experta d’una vintena llarga d’investigadors i clínics d’arreu dels Estats Units semblava donar-li la raó, però no del tot. Des dels anys 50 del segle passat fins gairebé l’any 2000, l’arsenal terapèutic havia crescut a raó d’un únic fàrmac per dècada. I en cap cas assegurava la curació. Els anys 2000 arrancaven, però, amb almenys mitja dotzena de medicaments amb menys efectes adversos i expectatives molt millors. Alguna cosa bona estava passant.
Gairebé vint anys després, aquella petita revolta farmacològica està a punt de transformar-se en una revolució. “Estan passant moltes coses i totes alhora”, descriu Josep Tabernero, director de l’Institut d'Oncologia Vall d'Hebron (VHIO), centre punter a Europa en assajos clínics avançats contra el càncer. En aquests moments hi ha un degoteig constant de nous fàrmacs i d’estudis en fases preliminars i avançades que apunten resultats prometedors. Les raons són diverses, però hi ha tres motius principals.
El primer és l’èxit de l’anomenada medicina de precisió. El seu objectiu és trobar molècules que ataquin proteïnes o vies específiques de les cèl·lules d’un tumor en la funció de les quals es vol interferir, habitualment maligna. Com més específiques siguin aquestes molècules, més personalitzada serà la teràpia. És un camp del qual “ja en sabem molt”, diu Tabernero. El segon punt fa referència a la immunoteràpia, que tot i la seva “joventut”, ja ofereix resultats en forma de fàrmacs i promeses realistes de nous medicaments. El tercer és l’estudi de la metàstasi, un procés biològic conceptualment complex i que en molts aspectes continua sent un trencaclosques de molt mal solucionar.
El futur immediat
“No hi haurà mai una sola forma de càncer que sigui rellevant per a un alt nombre de pacients”, assenyala Tabernero. Això és així perquè no hi ha un únic factor, sigui genètic o molecular, que sigui comú a totes les formes de càncer. La primera derivada d’aquesta constatació és que fàrmacs que actuen sobre un 15% o un 20% dels tumors són tot un èxit. “Fins als anys 80 només teníem una sola forma de càncer de mama; avui en tenim més de deu”, afegeix. La nova realitat ha obligat les principals agències reguladores –FDA als Estats Units, EMA a Europa– a canviar els criteris per aprovar nous fàrmacs. Fa poc més d’una dècada només s’aprovaven fàrmacs que eren actius en un gran nombre de pacients. Ara el que es busca són medicaments que són actius per a grups més reduïts de malalts, grups en què domina una variant d’un tumor, com ho seria una de les formes de càncer de mama.
“Ara tenim molt més coneixement de la malaltia i de les seves vulnerabilitats”, exposa el director del VHIO. El coneixement es tradueix en millors pronòstics i millors tractaments. I també en línies estratègiques de recerca dels grans centres del món. Un document publicat pel Memorial Sloan Kettering Cancer Center de Nova York (MSKC) marca com a objectiu assolir una medicina personalitzada “amb tractaments que coincideixen amb la nostra genètica i la nostra història personal”. És a dir, teràpies individualitzades que prometen ser més efectives i causar menys efectes secundaris que les quimioteràpies que s’administren a un pacient mitjà. L’objectiu es podria plantejar des de qualsevol centre avançat del món.
El mateix passa amb la recerca en immunoteràpia. El gran objectiu és que sigui el mateix organisme el que faci front a les cèl·lules malignes del càncer a partir de l’acció del sistema immunitari. “Tothom té un sistema immunitari, una maquinària llesta per lluitar”, rebla Tabernero. El problema és que aquest principi és vàlid només per al 25% dels tumors. I, a més, el tumor “es defensa” i “atura la maquinària” defensiva, de manera que la immunitat deixa de ser efectiva. Els medicaments actualment disponibles miren de “despertar” la maquinària que “estava adormida però educada per lluitar contra el tumor”. Són els inhibidors de punts de control o checkpoints, adreçats sobretot a enfortir les capacitats de les cèl·lules T del sistema immunitari. “Activen i reforcen el nostre sistema de defenses”, aclareix el director del VHIO. De llarg, aquesta és la línia de desenvolupament amb un nombre més gran de candidats a nous fàrmacs que centres de recerca i empreses farmacèutiques tenen a la vista.
Una segona estratègia d'immunoteràpia consisteix en la manipulació de les cèl·lules T d'un pacient amb l’objectiu d’atacar més fàcilment les cèl·lules canceroses. És el que s’anomena teràpia de receptor d'antigen quimèric, o teràpia CAR-T. Les cèl·lules T es recullen de la sang d'un pacient, es redissenyen genèticament per reconèixer certes proteïnes de les cèl·lules canceroses i es tornen a introduir al torrent sanguini del pacient. "Estem creant fàrmacs vius", exclama Michel Sadelain, director del Centre d'Enginyeria Cel·lular de MSKC. Bàsicament, es trasplanten cèl·lules vives als pacients. En una situació ideal, haurien de donar millor resultat que qualsevol producte químic.
Propietats distintives
Que no hi hagi un factor o una característica comuna a tots els tumors no vol dir que no existeixin “propietats distintives” de les cèl·lules canceroses a partir de les quals es pugui orientar estratègies de recerca o línies específiques. Robert Weinberg, investigador del departament de biologia del MIT, i Douglas Hanahan, director de l’Institut de Recerca Experimental del Càncer a l’Escola Politècnica de Suïssa, són els autors d’una proposta de classificació que ha estat acceptada universalment i que descriu quines són les propietats o els segells distintius de les cèl·lules de qualsevol tumor. La llista és de gran ajut tant per a científics com per a la indústria.
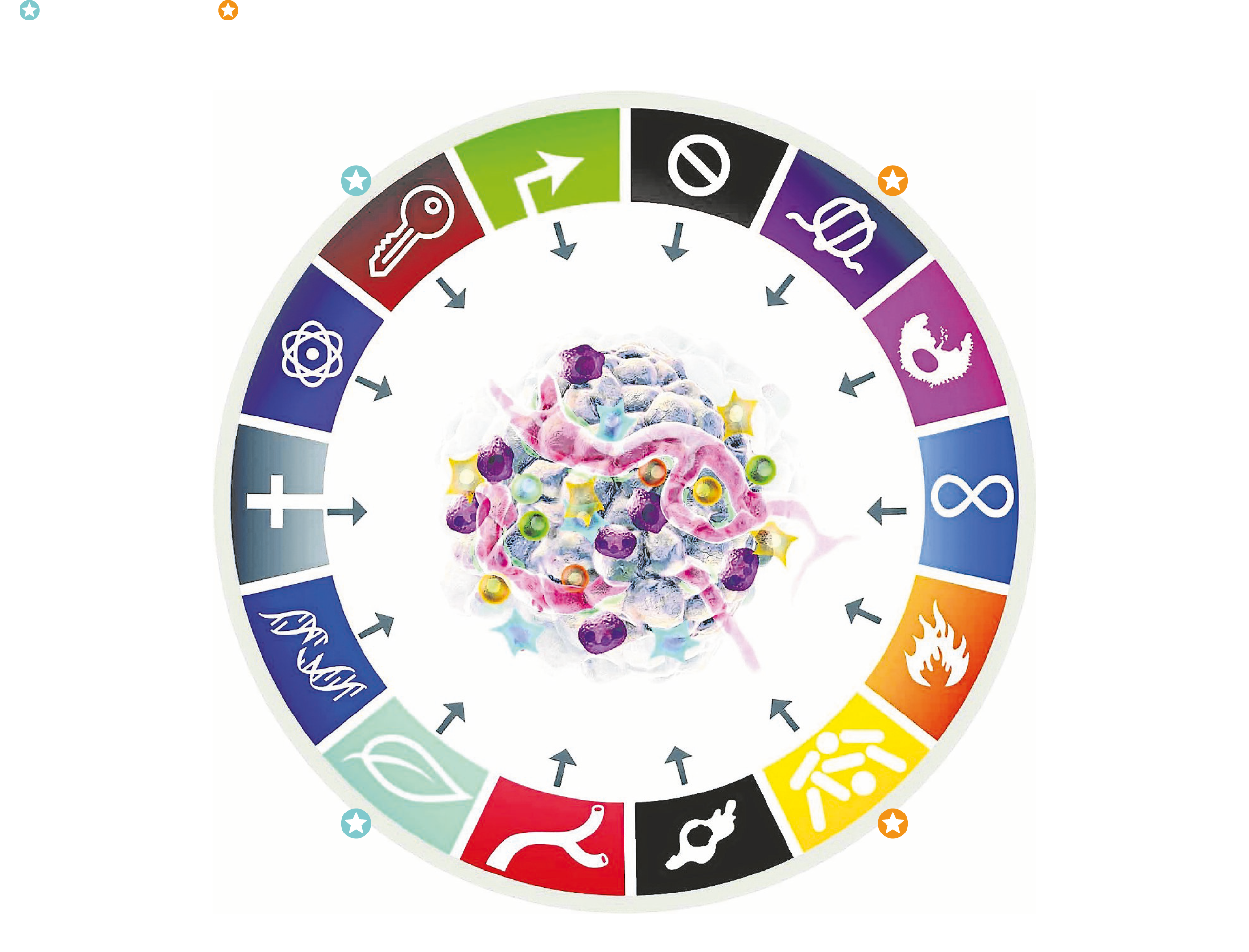
En la primera versió, publicada l’any 2000, els investigadors van proposar 6 propietats distintives amb les quals volien agrupar de manera comprensible les “capacitats i característiques adquirides” de les cèl·lules que propicien l’origen i el creixement dels tumors i la seva expansió, com per exemple les vinculades a la divisió cel·lular.
De 6 propietats es va passar a 8 l’any 2011, amb l’afegit de dues “propietats habilitants”. Són la proliferació cel·lular excessiva; la capacitat d’esquivar les hormones supressores del creixement; evitar la mort cel·lular; tenir activada de manera permanent la capacitat replicativa, cosa que converteix les cèl·lules en immortals; induir la formació de vasos sanguinis per nodrir els tumors; l’activació de la metàstasi; la reprogramació del metabolisme cel·lular, i fer-se invisible a l’acció del sistema immunitari. Dit d’una altra manera, les cèl·lules es divideixen sense parar, creixen més del normal, es converteixen en immortals i preparen el camí per a la metàstasi. Els dos articles, els de l’any 2000 i 2011, consten encara en la reduïda llista dels més citats a la revista Cell, un dels grans referents mundials en biologia.
El gener del 2022 Weinberg i Hanahan publiquen una tercera revisió a la revista Cancer Discovery, de l’Associació Americana per a la Recerca en Càncer (AACR). Com a novetat hi afegeixen dues propietats distintives més –la inestabilitat genòmica i l’impacte dels fenòmens inflamatoris– i quatre propietats habilitants més: la plasticitat cel·lular, la reprogramació epigenètica, la influència del microbioma i la senescència cel·lular. És a dir, l’alteració de cromosomes i gens, els canvis induïts per la inflamació en el microambient de la cèl·lula, la influència genètica de la gran quantitat de microorganismes que conviuen amb nosaltres, i les respostes al dany cel·lular.
Molt probablement, admet Hanahan en un comentari editorial, el temps farà que aquestes propietats es consolidin o bé siguin bescanviades per altres de més generals. “Les vuit primeres propietats distintives i les dues habilitants han perdurat en el temps”, escriu. D’elles “se sap gairebé tot”. En canvi, de les afegides a l'última revisió encara s’està a les beceroles i són moltes les coses que “poden canviar”. Amb l’epigenètica, les cèl·lules mare del càncer o la senescència cel·lular tot just ara comencen a donar resultats rellevants.
“En teoria són principis generals, però no són en absolut inamovibles”, puntualitza Tabernero. Posa com a exemple el cas del microbioma (bacteris, virus i fongs que tenim al cos i condicionen la salut), que ha anat canviant en el decurs del temps. “Ara sabem que és fonamental tant per la gènesi dels tumors com en la resposta als medicaments”. La seqüenciació del genoma del microbioma ens explica que almenys tenim 4.000 espècies diferents de bacteris i altres microorganismes que viuen en equilibri al nostre cos i que la gran majoria hi són perquè s’han incorporat i adaptat al llarg de l’evolució. La suma de tots determina una capacitat de generar proteïnes beneficioses “enorme”, però canvis en la dieta, l’ús excessiu d’antibiòtics i altres factors poden fer que hi hagi un “excés de bacteris equivocats” que afavoreixin l’aparició de tumors.
El conjunt de propietats distintives també orienten la recerca. Indiquen allò que és tendència tant al sector públic com sobretot a la indústria. Saber que s’investiga en cèl·lules mare del càncer o senescència cel·lular, posem per cas, obre expectatives per al desenvolupament de teràpies. Per tant, fer-hi recerca pot obrir amb més facilitat les portes del finançament. És en aquest marc que entren la seqüenciació massiva i el big data, els organoides i els anticossos monoclonals, totes eines fonamentals en la recerca actual del càncer. La immunoteràpia, la intervenció precoç o les biòpsies líquides seran complements clínics essencials.